美藥廠研發疫苗有進展 將展開更大規模臨床測試
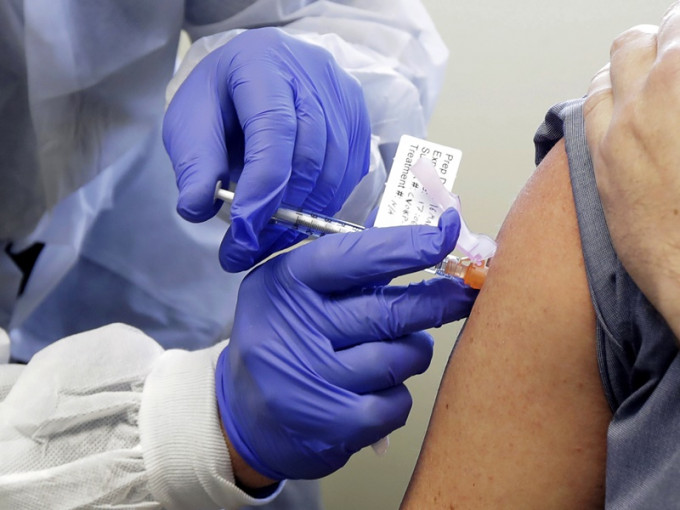
2020-05-19 13:51美國的新冠肺炎累計死亡病例周一突破9萬宗,確診病例則突破150萬宗。美國生物科技大廠莫德納公司(Moderna Inc.)發表報告,指首階段臨床試驗結果正面,首批8名志願者在3月接種疫苗後,產生抗體,測試同時證實疫苗安全,即將展開第2及第3階段更大規模的臨床測試。
莫德納表示,這種mRNA-1273的疫苗似乎在8名接受測試者體內產生抗體,具有免疫反應,且免疫程度與在新冠肺炎感染者體內觀察到的相同。受到消息刺激,道瓊斯工業平均指數全日大升逾911點。總統特朗普歡迎有關消息,形容該公司的研究難以置信,已看到成果,而市場亦因此大升。
該公司是於3月開始進行疫苗人體實驗,年齡介乎18至55歲。《紐約時報》說,儘管今次實驗人體樣本數量較少,但市場從中看到快速研發出新冠疫苗的希望,這足以推動股市上升。受利好消息影響,莫德納公司股價當天上漲近兩成。
全球目前超過100款候選疫苗正在研發,至少有8款展開人體試驗,mRNA-1273是其中之一。在莫德納第一階段的臨床實驗中,45名臨床試驗參與者在注射候選疫苗後,體內全都產出新冠病毒抗體。
在臨床實驗中,受試者分為3組,每組15人,注射的疫苗劑量各為25微克、100微克或250微克,注射完第一劑後,相隔28天再注射第2劑。
研究發現,實驗進行到第43天,即注射第2劑兩周後,25微克小組的血液樣本檢測出的結合抗體數量,跟已從新冠肺炎復原者抗體量相同。100微克小組血中的抗體數量更「遠超過」復原者。
不只如此,這款疫苗也讓至少8名受試者體內產生能對抗新冠病毒的中和抗體。
莫德納候選疫苗的第2階段試驗已經獲得美國食品及藥物監督管理局許可,將對600人進行測試,即將在本季度展開。至於最大規模及最重要的第3階段則會在7月展開。
莫德納最近才剛跟瑞士藥廠Lonza締結為期10年的合作關係,加快候選疫苗生產。莫德納行政總裁邦塞爾(Stephane Bancel)表示,希望最快7月就可以開始生產候選疫苗。他說:「我們的團隊只要一取得許可,就會開始作業。」他並說,跟Lonza合作後,每年的疫苗產能上看1億劑。







最新回應