美國周四審批輝瑞疫苗 文件顯示符合緊急授權使用
2020-12-09 09:43 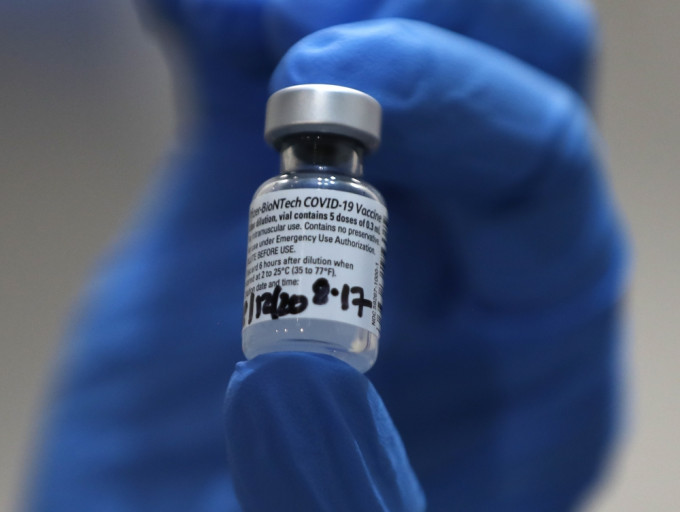
美國輝瑞藥廠參與研發的新冠疫苗,周二開始在英國大規模接種,美國食品藥品監督管理局(FDA)將於周四召開外部專家會議,討論是否批准緊急使用輝瑞與德國BioNTech合作研發的新型冠狀病毒疫苗,當局指最快在數日內作決定。
據當局公布文件顯示,疫苗的有效性數據符合緊急授權使用的預期,數據表明民眾接種第一劑疫苗後,已獲得部分保護,曾經感染新冠病毒的人,接種後亦會得益。文件同時指出,專家將會討論是否建議對16歲或以上人士接種。
有分析認為,當局公開的文件表明,疫苗將會獲批准。亦有專家說,這款疫苗看起來最少在短期內都是安全。
紐約市長白思豪就對輝瑞疫苗獲批充滿信心,指紐約市下星期就會獲得疫苗,形容對抗病毒終於來到最後階段。
輝瑞與德國夥伴上個月表示,他們研發的疫苗,有效率達95%,而且無重大安全問題。另一款由莫德納藥廠研製的新冠疫苗,就會在下星期提交FDA審批。另外,英國牛津大學與阿斯利康合作研發的新冠疫苗,第三階段試驗證實有效率約為70.4%,但如果調整劑量,第一針注射一半劑量,第二針全量的話,有效率能提升至90%。
分析指,牛津疫苗的有效性雖然不及輝瑞和莫德納,但價錢就較便宜,而且儲存更加方便,更容易運送到世界各地。
關鍵字








最新回應